Chemische eigenschappen van elementen van groep 2 en groep 7 (17)
- chemie
- 17 - 18 jaar
- 3e graad secundair
- 4h20
STEMgebied:
Graad:
Leeftijd studenten:
Tijd:
voorbereidingstijd:
lestijd:
leermethodologie
De les zal zowel praktisch als klassikaal zijn, de leerlingen krijgen videolinks met verkennende vragen ter voorbereiding van deze uitgebreide praktische activiteit, die uit 4 lessen bestaat. De les wordt praktisch uitgevoerd, maar de verkennende vragen moeten door de student volledig beantwoord en begrepen worden voordat hij aan het praktische onderzoek begint.
sleutelbegrippen:
Atoomstructuur en hoe de chemische eigenschappen van elementen afhangen van hun atoomstructuur, en in het bijzonder van de rangschikking van elektronen rond de kern.
De studenten bekijken de tendensen en reacties van de elementen van groep VII in detail. Deze praktische activiteiten stellen de studenten in staat de belangrijke kwantitatieve technieken te ontwikkelen. Zij krijgen ook inzicht in analytische proeven, waardoor de studenten ervaring kunnen opdoen met kwalitatieve praktische vaardigheden zoals waarneming.
Overview
Voer de praktische opdrachten met betrekking tot groepschemie uit en bespreek de overeenkomsten en verschillen in de chemische eigenschappen van de groepen 2 en 7.
Student mission
U bent een wetenschapper die in een forensisch laboratorium werkt. Er zijn monsters van onbekende anorganische materialen verzameld uit een fabriekspakhuis nadat het in brand was gevlogen. De politie denkt dat de brand is aangestoken en u heeft de opdracht gekregen ze te analyseren. Je moet bepalen wat de onbekende materialen zijn, gebaseerd op hun reactiviteit. U bent verantwoordelijk voor de materiaalanalyse.
Uw taken zijn: Bepaal de chemische reactiviteit van de onbekende materialen.
21st century technical skills gained through this activity
Lijst van vaardigheden:
∙ Probleemoplossend vermogen,
∙ Praktische analyse,
∙ Kritisch denken,
∙ Conclusies trekken op basis van feiten,
∙ Onderzoekend leren.
Related job roles
Forensisch Wetenschapper
Forensisch onderzoeker
Chemisch analist
Differentiation strategies to meet diverse learning needs
Peer Mentoring, praktische taken, vragen formuleren.
Lesson plan
Vier lessen van 45 minuten (Als uw lessen korter of langer zijn, kunt u deze reeks in meer of minder lessen opsplitsen).
Time to complete Lesson
Groep 2: metalen
∙ Ken het uiterlijk van de elementen van groep 2 en weet dat de metalen verderop in de groep in olie moeten worden bewaard.
∙ Ken ook hun fysische en chemische eigenschappen die in de onderstaande tabel staan vermeld. ∙ Weten dat vlamtesten worden gebruikt om metaalkationen te identificeren en ook het bestaan van elektronenschillen aantonen.
Fysische eigenschappen:
- weten dat het goede geleiders zijn van elektriciteit.
- weten dat ze een lage dichtheid hebben.
- Weten dat ze een grijs glanzend oppervlak hebben als ze vers gesneden zijn met een mes.
Chemische eigenschappen:
- weten dat ze ionische verbindingen vormen met niet-metalen.
- Weten dat het zeer reactieve metalen zijn.
Groep 7(17): halogenen
De trends in de reactiviteit van de halogenen kunnen worden verklaard door hun bereidheid om elektronen van andere soorten te aanvaarden.
Expected Learning Outcomes
Tendensen in atoomstraal, tendensen in ionisatie-energie, groepen en perioden, kernlading.
Prior knowledge and vocabulary
Geef de leerlingen de print van het model voor wetenschappelijk onderzoek en het sjabloon Test je idee om hen te helpen met hun onderzoeksvraag. Zie bijlage I. en II.
Science and Engineering/Math Practices
Groep 2: metalen
Eenheid AS 1: Basisbegrippen in de natuurkundige en anorganische scheikunde
1.10 Kwalitatieve testen:
1.10.3 Kationen testen gebruiken, inclusief:
– Vlamtests om de metaalionen Li+, Na+, K+, Ca2+, Ba2+ en Cu2+ te identificeren
Eenheid AS 2: Verdere fysische en anorganische scheikunde en een inleiding tot de organische scheikunde
2.11 Elementen van groep II en hun verbindingen
2.11.1 Uitleggen waarom deze als s-blok elementen worden beschouwd;
2.11.3 De reacties van de elementen met zuurstof, water en verdunde zuren onderzoeken en beschrijven;
2.11.4 De basische aard van de oxiden en hun reacties met water en verdunde zuren beschrijven;
De leerresultaten zijn afgestemd op bovengenoemd leerplan.
∙ Ken het uiterlijk van de elementen van groep 2 en weet dat de metalen verderop in de groep in olie moeten worden bewaard.
∙ Ken ook hun fysische en chemische eigenschappen die in de onderstaande tabel staan vermeld. ∙ Weten dat vlamtesten worden gebruikt om metaalkationen te identificeren en ook het bestaan van elektronenschillen aantonen.
Fysische eigenschappen:
- weten dat het goede geleiders zijn van elektriciteit.
- weten dat ze een lage dichtheid hebben.
- Weten dat ze een grijs glanzend oppervlak hebben als ze vers gesneden zijn met een mes.
Chemische eigenschappen:
- weten dat ze ionische verbindingen vormen met niet-metalen.
- Weten dat het zeer reactieve metalen zijn.
Groep 7(17): halogenen
Weten dat de trends in de reactiviteit van de halogenen verklaard kunnen worden door hun bereidheid om elektronen van andere soorten te accepteren.
Dit leerresultaat is afgestemd op het CCEA GCE Chemistry curriculum:
Eenheid AS 1: Basisbegrippen in de natuurkundige en anorganische scheikunde
1.8 Halogenen
1.8.5 De tendens in het oxiderend vermogen van de halogenen naar beneden toe beschrijven, toegepast op de verdringingsreacties van de halogenen met andere halide-ionen in oplossing;
1.10 Kwalitatieve proeven
1.10.4: Toevoegen van aangezuurde zilvernitraatoplossing om onderscheid te maken tussen chloride, bromide en jodide (gevolgd door toevoegen van verdunde en geconcentreerde ammoniakoplossing)
Curriculum Alignment
Lesbegin: De leerkracht helpt de leerlingen na te denken over wat ze al weten en eventuele hiaten in hun kennis te identificeren. Het is belangrijk de belangstelling voor de komende concepten te stimuleren, zodat de leerlingen klaar zijn om te leren. De leerkracht kan de leerlingen de opdracht geven openingsvragen te stellen of op te schrijven wat ze al weten over het onderwerp. Dit is ook het moment waarop het concept voor het eerst aan de leerlingen wordt voorgesteld.
De leerlingen krijgen deze videolinks voor de les, volgens de flipped classroom-strategie die wordt toegepast. De leerlingen bekijken de video’s thuis, beantwoorden de vragen die bij de video’s horen. Ze zullen ook hun eigen vragen en ideeën formuleren, dus onderzoeken ze de praktische onderzoeken die ze hebben geobserveerd en stellen ze onderzoekende vragen aan de docent, terwijl ze ook de vragen beantwoorden die ze eerder hebben gekregen. Het stellen en beantwoorden van vragen en het formuleren van ideeën zal de leerling een beter inzicht geven in de praktische activiteiten die hij zal uitvoeren. Als ze de proefjes hebben uitgevoerd, moeten de leerlingen conclusies trekken op basis van de resultaten om te zien of deze conclusies overeenstemmen met de hypothese die ze vóór de experimenten hebben opgeschreven.
Materialen: videolinks, aantekeningen met vragen
1e les:
- https://www.youtube.com/watch?app=desktop&v=O6DaCYKh77E
- https://www.youtube.com/watch?app=desktop&v=dKCHnuEdVY8
- https://www.youtube.com/watch?v=HW2jRyQ3dzo
2e les:
3e les:
4e les:
- https://www.youtube.com/watch?v=J7b2aBKa6-U
- https://www.youtube.com/watch?app=desktop&v=7F4JhrBWdY4
voorbereiding: [ 20] Minuten
Begeleiding van de leerervaring: [10] Minuten
overgang: [ 2] Minuten
De leerkracht zal: de vraag- en antwoordsessie leiden, aan het begin van elke les het concept uitleggen.
Leerlingen zullen: aandachtig luisteren, notities nemen en vragen stellen
Verkennen: Tijdens de verkenningsfase verkennen de leerlingen actief het nieuwe concept door middel van concrete leerervaringen. Zij kunnen worden gevraagd de wetenschappelijke methode te doorlopen en met hun medeleerlingen te communiceren om waarnemingen te doen. Deze fase stelt leerlingen in staat om te leren op een praktische manier.
Materialen: Praktische uitrusting en chemische analyses
Begeleiding van de leerervaring: [30] Minuten
De leerkracht zal: De praktijkles begeleiden, de leerlingen instructies geven en hen bewust maken van gezondheid en veiligheid met betrekking tot hun oefeningen:
1e les:
- vlamtest – praktisch in het lab
2e les:
- kijken naar de metalen in groep 2 en onderzoeken hoe reactief ze zijn – praktisch in het lab
3e les:
- reacties met elementen uit groep 2 en groep 7 – praktisch in het lab
4e les:
- Verdringingsreacties van de halogenen met andere halogenide-ionen in oplossing en toevoeging van aangezuurde zilvernitraatoplossing om onderscheid te maken tussen chloride, bromide en jodide (gevolgd door toevoeging van verdunde en geconcentreerde ammoniakoplossing) – practisch in het lab
Studenten zullen: Hun opdrachten op een veilige en accurate manier uitvoeren, hun opdrachten en instructies grondig lezen en begrijpen voor ze starten.
uitlegfase: Dit is een door de leraar geleide fase die leerlingen helpt nieuwe kennis te synthetiseren en vragen te stellen als ze meer verduidelijking nodig hebben. Om de uitlegfase effectief te laten zijn, moeten docenten leerlingen vragen om te delen wat ze tijdens de verkenfase hebben geleerd, voordat ze technische informatie op een meer directe manier introduceren. Dit is ook het moment waarop leerkrachten video, computersoftware of andere hulpmiddelen gebruiken om het begrip te vergroten.
Als de leerlingen tijdens de praktische oefeningen al moeilijkheden hebben, kan de leerkracht dan ook al de extra uitleg of hulp bieden.
Materialen: labo-uitrusting
voorbereiding: [30] Minuten
begeleiding van de leerervaring: [5 – 10] Minuten
overgang: [ 0] Minuten
de leerkracht zal: De concepten en/of technieken in het lab verder uitleggen.
de leerlingen zullen: Aandachtig luisteren.
Uitwerken: Deze fase richt zich op het geven van ruimte aan leerlingen om toe te passen wat ze hebben geleerd. Dit helpt hen om een dieper begrip te ontwikkelen. Leerkrachten kunnen leerlingen vragen om presentaties te maken of extra onderzoeken uit te voeren om nieuwe vaardigheden te versterken. Deze fase geeft leerlingen de kans om hun kennis te verstevigen voor de evaluatie.
Na elke les wordt de leerlingen gevraagd in groepjes te werken en het onderwerp meer in detail te onderzoeken. Vervolgens bereiden zij als huiswerk een presentatie voor en leren zij de klas een ander aspect van het praktijkgedeelte.
Materialen: Powerpoint, notities
voorbereiding: [60 ] minuten voor de leerlingen om research te doen en de slides voor te bereiden.
Begeleiding van de leerervaring: [ 10] minuten per groep om hun presentatie voor te stellen.
overgang: [ 0] Minuten
de leerkracht zal: De presentaties van de studenten evalueren en eventuele bijvragen stellen.
Studenten zullen: de presentatie voorstellen aan de rest van de groep, eventuele bijvragen beantwoorden.
Evalueren: Tijdens deze fase kunnen leerkrachten hun leerlingen observeren en zien of zij de kernconcepten volledig begrijpen. Het is ook nuttig om op te merken of leerlingen problemen op een andere manier benaderen op basis van wat ze hebben geleerd. Andere nuttige elementen van de Evaluatie zijn zelfevaluatie, peer-assessment, schrijfopdrachten, en examens.
De leerlingen krijgen aantekeningen met vragen na het practicum en weblinks naar chemiesites om het inzicht van de leerlingen in de praktische onderwerpen te vergroten.
De ondervraging na het praktijkgedeelte kan tot het volgende lesuur worden uitgesteld, indien uw tijd tijdens het praktijkgedeelte overschreden wordt.
Leerlingen kunnen ook een toets OF tijdgebonden opdrachten krijgen.
Materialen: test of tijdgebonden opdracht
voorbereiding: [ 10 ] Minuten
begeleiding van de leerervaring: [5] Minuten voor extra vragen te stellen.
[45 -60 ] Minuten voor de test of de tijdgebonden opdracht
Overgang: [ 0 ] Minuten
De leerkracht zal: de leerlingen naar bronnen leiden om hun begrip te vergroten OF de leerlingen een tijdgebonden evaluatie voorleggen op basis van hun bevindingen
De studenten zullen: de vragen beantwoorden na het bekijken van de videolinks van de leerkracht OF de vragen zo volledig mogelijk beantwoorden in de toegewezen tijd.
Zelfstandige leertaken:
Voorzie 2-3 opdrachten die de leerlingen voor de volgende les moeten uitvoeren:
- De leerlingen zullen de videolinks bekijken die de leerkracht hen heeft gegeven om hun kennis te vergroten.
- De leerlingen onderzoeken toepassingen in het echte leven van wat ze in de klas geleerd hebben.
- De leerlingen beantwoorden vragen na de les
- De leerlingen zullen in groepjes werken aan de voorbereiding van presentaties en deze presenteren aan hun klas
Lesson
Studenten krijgen tijdig één op één feedback. De feedback zal verwijzen naar de resultaten van de toetsing en of de leerling aan die resultaten voldoet. Er zal ook rekening gehouden worden met de feedback van de leerling over hoe hij de les vond.
Student feedback
De kennis die in deze les wordt opgedaan, kan worden afgezet tegen de atoomstructuur in de AS/A2-natuurkunde en de rol van biologisch beschikbare metalen in de AS/A2-biologie.
Curriculum mapping of outcomes attained
Praktische test, presentatie door de studenten, tijdsgebonden evaluatie en vraag en antwoord.
Materials
Dit lesplan zal vergezeld gaan van een volledige praktische instructie voor de lessen, hieronder volgt slechts een samenvatting.
Halogeenverbindingen fluoride, chloride, bromide en jodide
Natriumchloride
Natriumbromide
Natriumjodide
Verdunde en geconcentreerde ammoniakoplossing
Reageerbuizen
Rekjes voor reageerbuizen
Metalen pincet
Waterbak
Bunsenbrander
Retort Statieven
Zilvernitraat
Natriumbromide
Natrium Jodide
Verdund salpeterzuur
Nichroom draad lus
Verdund zoutzuur
Li+, Na+, K+, Ca2+, Ba2+ en Cu2+ (metaalzouten)
Gedestilleerd water
Chloorwater
Broomwater
Jodiumhoudend water
Zilverfluoride
Zilverchloride
Zilverbromide
Zilverjodide
Ammoniak
Metalen van groep 2
Zuurkasten
Brillen
Laboratoriumjassen
Handschoenen
Preparation
De studenten moeten de aangeboden videolinks bekijken en de vragen in hun aantekeningen proberen; de student moet zelf vragen beantwoorden om na te gaan of de studenten de concepten begrijpen voordat hij aan het practicum begint.
Team Work
De leerlingen werken in teams om de onderwerpen te onderzoeken en een presentatie voor de klas voor te bereiden over elk van de experimenten. Dit is een uitbreiding van de basiskennis, waarbij de leerlingen meer moeten onderzoeken over de conclusies die zijn getrokken uit de praktische activiteiten.
Rubrics
| Schaal van zelfstandigheid | ||||
| Niet zelfstandig | Veel hulp met een beetje zelfstandigheid | Zelfstandigheid met hier en daar een beetje hulp | Volledige zelfstandigheid | |
| De leraar geeft de leerlingen een volledige methode met duidelijke instructies voor het uitvoeren van de experimenten. | De leraar geeft de leerlingen een
schema voor de procedure, maar laat opties* toe bij verschillende stappen. De docent geeft de leerlingen een overzicht van de procedure om de experimenten uit te voeren, maar met enkele opties in techniek en uitrusting |
De leraar specificeert de samenstelling en concentratie van de oplossing. De leerlingen onderzoeken de methode om de bereiding van het experiment uit te voeren. Studenten onderzoeken methoden om de experimenten uit te voeren met behulp van de appartuur. | De leerlingen kiezen de chemische stof en de concentratie die gemaakt moet worden. Leerlingen onderzoeken methoden voor het uitvoeren van het experiment en kiezen de methode, chemicaliën en appartuur. | |
| Observatie en beoordeling van bekwaamheden. | ||||
| Het volgen van schriftelijke en mondelinge procedures. | De studenten volgen geschreven en gesproken instructies. | De studenten volgen geschreven en gesproken instructies en maken individuele keuzes bij het uitvoeren van het experiment | De leerlingen volgen een onderzochte methode | De leerligen onderzoeken een methode en volgen deze. |
| De materialen veilig gebruiken. | De leerlingen gebruiken de materialen veilig na een uitleg. | De leerlingen weten hoe ze de materialen veilig moeten gebruiken. | De studenten minimaliseren de risico’s met een minimale aansporing. | De studenten kennen de risico’s en minimaliseren deze. |
| Verslagen maken van de waarnemingen en de resultaten. | De studenten registreren de resultaten op een aangeleerde manier. | De studenten registreren de resultaten op een aangeleerde manier. | De studenten noteren nauwkeurige en precieze gegevens, methodisch en met een passend voorbeeld. | De studenten kiezen de meest doeltreffende manier om de gegevens op een nauwkeurige en specifieke manier weer te geven. |
| Onderzoek en presentatie | De gegevens worden gerapporteerd en conclusies worden getrokken. De studenten maken en presenteren een presentatie met veel begeleiding. | De gegevens worden gerapporteerd en conclusies worden getrokken. De studenten vergelijken de resultaten en geven een reden voor de verschillen. Ze maken en presenteren hun presentatie met enige begeleiding. | De studenten onderzoeken beschikbare methoden. Ze vergelijken de resultaten en rapporteren over de verschillen. Geschikte software wordt gebruikt om gegevens te verwerken. De studenten maken en presenteren hun presentatie met minimale begeleiding. | De studenten onderzoeken alternatieve manieren om hun werk te plannen. In hun rapportering zit planning, uitvoering en analyse van de resultaten. Er werd passende software gebruikt om gegevens te verwerken. Ze maken en presenteren hun presentatie zonder begeleiding. |
| Toepassen van onderzoeks-methoden bij het gebruik van instrumenten en apparatuur. | De leerlingen maken correct gebruik van de juiste apparatuur. Ze moeten de procedure nog volgen. | De studenten maken correct gebruik van de apparatuur. Ze moeten de procedure nog volgen. Methodisch geschikte variabelen werden geïdentificeerd, gemeten en gecontroleerd. | De leerlingen selecteren de geschikte apparatuur en gebruiken deze correct. Procedurele stappen moeten goed opeenvolgend zijn en waar nodig aangepast worden. Methodisch geschikte variabelen worden geïdentificeerd, gemeten en gecontroleerd. | De studenten kiezen geschikte apparatuur en technieken en gebruiken deze correct. De geschikte variabelen worden geïdentificeerd, gemeten en gecontroleerd. |
Naam:—————— Vak:————- Experiment: ————-
| Criteria | 4 Excellent (10 – 8 punten) | 3 Goed (7 – 6 punten) | 2 voldoende (5 – 4 punten) | 1 onvoldoende (3 – 0 marks) | Score |
|
Samenvatting |
Goed ontwikkelde beknopte verklaring van resultaten en methoden, inclusief alle belangrijke onderdelen van het experiment met resultaten. Vakkundig geschreven en duidelijk vermelde conclusies van het experiment. | De samenvatting bevat een beknopte uiteenzetting van resultaten en methoden, inclusief de meeste aspecten van het experiment, maar sommige details ontbreken of de resultaten en/of conclusies worden niet duidelijk vermeld. | De samenvatting mist een aspect van het experiment en/of resultaten
en/of conclusies. Over het geheel genomen zijn de belangrijkste aspecten van het verslag opgenomen en zijn de resultaten nauwkeurig. |
Een aantal onderdelen van het experiment ontbreken.
De student begrijpt niet hoe een samenvatting moet worden geschreven. Resultaten worden niet volledig getoond, en er worden geen conclusies getrokken. |
|
| opmerkingen: | |||||
|
Theorie |
Een overtuigend, vakkundig geschreven theoriegedeelte met de juiste wetenschappelijke bronnen om een context te geven voor de praktische activiteit en met uitleg om de relevante wetenschappelijke
principes. Chemische reacties worden duidelijk uitgelegd. Verwijzing naar relevante literatuur. |
De theorie wordt gepresenteerd, maar er worden geen geschikte wetenschappelijke bronnen bij vermeld; de theorie vormt de achtergrond voor de praktische activiteit en er wordt meer gebruik gemaakt van beschrijving dan van uitleg om de relevante wetenschappelijke beginselen in detail te beschrijven. Chemische reacties worden uitgelegd. De verwijzing naar relevante literatuur is onduidelijk. | De theorie wordt gepresenteerd, maar er worden geen geschikte wetenschappelijke bronnen vermeld en de achtergrond voor de praktische activiteit is beperkt. De relevante wetenschappelijke principes worden opgesomd en beschreven. Chemische reacties worden vermeld maar niet verklaard. De verwijzing naar relevante literatuur is onduidelijk en sommige delen ontbreken. | De theorie mist achtergrond en passende wetenschappelijke bronnen.
Chemische reacties worden niet vermeld. Er worden geen referenties gegeven. |
|
| Opmerkingen: | |||||
| Material/methodes | Goed geschreven methode. Alle materialen zijn vermeld. De methode is op een overtuigende, competente manier geschreven. De methode moet duidelijk zijn voor iedereen die hem leest, ook voor medeleerlingen. | De methode is goed geschreven en alle materialen zijn vermeld. Peers zijn in staat de methode te volgen. | De methode wordt beschreven. Sommige materialen worden niet genoemd. Peers kunnen de methode volgen, maar er kunnen enkele leemtes zijn. | De methode is niet beschreven en/of onjuist, leeftijdgenoten zijn niet in staat deze te volgen. Materialen zijn niet vermeld. | |
|
Data |
Alle figuren, grafieken en tabellen zijn
nauwkeurig gepresenteerd en voorzien van titels en/of bijschriften. Het gegevensgedeelte is goed georganiseerd en gemakkelijk te begrijpelijk. Alle berekeningen zijn nauwkeurig uitgevoerd. |
Alle figuren, grafieken en tabellen zijn
meestal accuraat en bevatten titels en/of bijschriften met één onvolledigheid. Het gegevensgedeelte is georganiseerd en gemakkelijk te begrijpen. Alle berekeningen zijn nauwkeurig uitgevoerd. |
De meeste figuren, grafieken en tabellen zijn nauwkeurig en bevatten titels en/of bijschriften met meer dan één
onvolledigheid. Het gegevensgedeelte is georganiseerd. Alle berekeningen zijn nauwkeurig ingevuld met enkele kleine fouten. |
Figuren, grafieken, tabellen bevatten fouten en/of zijn slecht opgebouwd. Titels en/of bijschriften ontbreken of zijn onjuist. De berekeningen zijn onjuist. | |
| Opmerkingen: | |||||
Ek
Bijlage. I.
Wetenschappelijk onderzoek
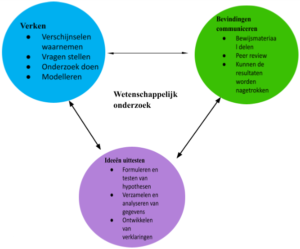
Bijlage. II.
Test je idee
Je vraag moet betrekking hebben op de gemanipuleerde variabele en de responsvariabele. |
|
Je hypothese moet geschreven worden als een “als, dan, omdat”-verklaring. |
|
|
|
Maak een lijst van je benodigdheden. |
|
Moet bevatten…
|
|
Geef je gegevens weer met behulp van geschikte grafieken en/of diagrammen. |
|
Geef aan of uw hypothese kan worden aanvaard of verworpen op basis van de waargenomen gegevens. |
|
Geef ideeën voor het herzien van je testidee of nieuwe gerelateerde ideeën om te testen. |
|
|
|
Bijlage. III.
Procedure vlamtest:
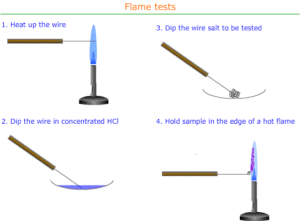
- Dompel een schone draadlus in een vast monster van de te testen verbinding.
- Steek de lus in de rand van de blauwe vlam van een bunsenbrander.
- Observeer en noteer de kleur van de vlam.
- Was de draadlus in verdund zoutzuur voor het inoculeren met het metaalzout.
Onderstaande tabel laat de vlamkleur zien voor zes vaak voorkomende metaalionen:
| Lithium | Rood |
| Natrium | Geel |
| Kalium | Lila |
| Calcium | Oranje-rood |
| Barium | Groen |
| koper | Blauw-groen |
Bijlage. IV.
De reactiviteit van metalen uit groep 2
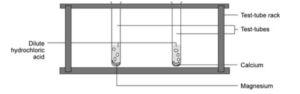
Procedure:
- Vul twee reageerbuisjes voor een kwart met verdund zoutzuur
- Laat in één reageerbuis een klein stukje magnesium vallen.
- In het andere laat je een stukje calcium vallen.
- Vergelijk de reactiviteit van de twee metalen.
- Laat nog een beetje magnesium in het eerste reageerbuisje vallen en zet je duim over het uiteinde.
- Wanneer de druk voelbaar is, haal je je duim eraf en test je het gas met een aangestoken splinter.
- Noteer wat er gebeurt.
Bijlage. V.
Calcium voorbereiden:

Procedure chloride:
Om calciumchloride voor te bereiden, moeten we onderstaande stappen volgen:
- Neem een bekerglas en doe er de kalksteen in met handschoenen aan tot het bekerglas voor een kwart gevuld is.
- Voeg nu HCl (zoutzuur) toe tot het even hoog staat als de kalksteen.
- Als het zoutzuur de kalksteen oplost, beginnen er luchtbellen te ontstaan. Meng nu voorzichtig de inhoud in het bekerglas en let er op dat de reactie volledig is. Als alle kalksteen is opgelost, voeg dan een beetje kalksteen toe.
- Filter vervolgens de vaste stoffen weg door de oplossing via filtreerpapier uit te gieten zodra de oplossing stopt met borrelen.
- Verwarm nu het tweede bekerglas, waarin zich een calciumchlorideoplossing bevindt. De vaste calciumchloride is datgene wat overblijft nadat het water verdampt is.
Bijlage. VI.
Procedure voor de verplaatsing van halogenen
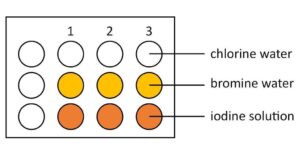
- Neem een reactieblad en etiketteer de rijen, Cl2, Br2, I2 en de kolommen H2O, NaCl, NaBr, NaL met een niet-permanente markeerstift of door het reactieblad boven op een stuk papier te leggen. Als alternatief kan dit experiment worden uitgevoerd op een gelamineerd exemplaar van de geïntegreerde instructies.
- Voeg met behulp van het pipetje 3-4 druppels van het chloorwater toe aan elk putje in de eerste rij.
- Doe hetzelfde voor broomwater in de tweede rij
- Doe hetzelfde voor de jodiumoplossing in de derde rij.
- Noteer de kleuren van elke oplossing
- Voeg 3-4 druppels gedestilleerd water toe en elk putje in de eerste kolom.
- Doe hetzelfde voor de natriumchlorideoplossing in de tweede kolom.
- Doe hetzelfde voor de natriumbromideoplossing in de derde kolom.
- Doe hetzelfde voor de natriumjodide-oplossing in de vierde kolom.
- Observeer en noteer de kleurveranderingen die in elke rij plaatsvinden door het eerste putje met de andere in de rij te vergelijken.
Toevoegen van aangezuurde zilvernitraatoplossing om onderscheid te maken tussen chloride, bromide en jodide (gevolgd door toevoegen van verdunde en geconcentreerde ammoniakoplossing)
Test op halide-ionen in een waterige oplossing.
Test op chloride-, bromide- en jodide-ionen in waterige oplossing Deze test moet in oplossing worden uitgevoerd. Als men uitgaat van een vaste stof, moet deze eerst worden opgelost in zuiver water.
De oplossing wordt aangezuurd door verdund salpeterzuur toe te voegen. (Onthoud: zilvernitraat + verdund salpeterzuur.) Het salpeterzuur reageert met, en verwijdert, andere ionen die ook een verwarrende neerslag met zilvernitraat zouden kunnen geven.
Procedure:
- Voeg aan een klein volume van elk van de oplossingen van kaliumchloride, kaliumbromide en kaliumjodide in drie afzonderlijke reageerbuizen een gelijk volume verdund salpeterzuur toe, gevolgd door ongeveer 2 cm3 zilvernitraatoplossing.
- Noteer je waarnemingen
- Wervel de buisjes om ervoor te zorgen dat de gevormde precipitaten in elk geval gelijkmatig verdeeld zijn en verdeel vervolgens de inhoud van elk buisje in tweeën.
- Voeg aan de ene helft van de inhoud een overmaat verdunde waterige ammoniakoplossing toe en observeer wat er gebeurt. Noteer uw waarnemingen.
- Voeg aan de andere helft, in een zuurkast, een overmaat geconcentreerde ammoniakoplossing toe en kijk wat er gebeurt. Noteer uw waarnemingen.

